ნახშირბადი
| ნახშირბადი |
| 6C |
| 12.011 |
| 2s2 2p2 |
 | ||||||||||||||||||||||||||||
| ზოგადი თვისებები | ||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| სტანდ. ატომური წონა Ar°(C) |
[12.0096, 12.0116] 12.011±0.002 (დამრგვალებული) | |||||||||||||||||||||||||||
| ნახშირბადი პერიოდულ სისტემაში | ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
| ატომური ნომერი (Z) | 6 | |||||||||||||||||||||||||||
| ჯგუფი | 14 | |||||||||||||||||||||||||||
| პერიოდი | 2 პერიოდი | |||||||||||||||||||||||||||
| ბლოკი |
| |||||||||||||||||||||||||||
| ელექტრონული კონფიგურაცია | [He] 2s2 2p2 | |||||||||||||||||||||||||||
| ელექტრონი გარსზე | 2, 4 | |||||||||||||||||||||||||||
ელემენტის ატომის სქემა | ||||||||||||||||||||||||||||
| ფიზიკური თვისებები | ||||||||||||||||||||||||||||
| აგრეგეგატული მდგომ. ნსპ-ში | მყარი სხეული | |||||||||||||||||||||||||||
| სუბლიმაციის ტემპერატურა |
3642 °C (3915 K, 6588 °F) | |||||||||||||||||||||||||||
| სიმკვრივე (ო.ტ.) |
ამორფული: 1.8–2.1 გ/სმ3 გრაფიტი: 2.267 გ/სმ3 ალმასი: 3.515 გ/სმ3 | |||||||||||||||||||||||||||
| სამმაგი წერტილი | 4600 K, 10 800 კპა | |||||||||||||||||||||||||||
| დნობის კუთ. სითბო | გრაფიტი: 117 კჯ/მოლი | |||||||||||||||||||||||||||
| მოლური თბოტევადობა |
გრაფიტი: 8.517 ჯ/(მოლი·K) ალმასი: 6.155 ჯ/(მოლი·K) | |||||||||||||||||||||||||||
| ატომის თვისებები | ||||||||||||||||||||||||||||
| ჟანგვის ხარისხი | −4, −3, −2, −1, 0, +1, +2, +3, +4 | |||||||||||||||||||||||||||
| ელექტროდული პოტენციალი |
| |||||||||||||||||||||||||||
| ელექტროუარყოფითობა | პოლინგის სკალა: 2.55 | |||||||||||||||||||||||||||
| იონიზაციის ენერგია |
| |||||||||||||||||||||||||||
| კოვალენტური რადიუსი (rcov) |
sp3: 77 პმ sp2: 73 პმ sp: 69 პმ | |||||||||||||||||||||||||||
| ვან-დერ-ვალსის რადიუსი | 170 პმ | |||||||||||||||||||||||||||
|
ნახშირბადის სპექტრალური ზოლები | ||||||||||||||||||||||||||||
| სხვა თვისებები | ||||||||||||||||||||||||||||
| მესრის სტრუქტურა |
ჰექსაგონალური  | |||||||||||||||||||||||||||
| მესრის სტრუქტურა |
აჟურული  | |||||||||||||||||||||||||||
| ბგერის სიჩქარე | ალმასი: 18 350 მ/წმ (20 °C) | |||||||||||||||||||||||||||
| თერმული გაფართოება | ალმასი: 0.8 µმ/(მ·K) (25 °C) | |||||||||||||||||||||||||||
| თბოგამტარობა |
გრაფიტი: 119-165 ვტ/(მ·K) ალმასი: 900-2300 ვტ/(მ·K) | |||||||||||||||||||||||||||
| კუთრი წინაღობა | გრაფიტი: 7.837 ნომ·მ | |||||||||||||||||||||||||||
| მაგნეტიზმი | დიამაგნეტიკი | |||||||||||||||||||||||||||
| მაგნიტური ამთვისებლობა | −5.9×10−6 სმ3/მოლ | |||||||||||||||||||||||||||
| იუნგას მოდული | ალმასი: 1050 გპა | |||||||||||||||||||||||||||
| წანაცვლების მოდული | ალმასი: 478 გპა | |||||||||||||||||||||||||||
| დრეკადობის მოდული | ალმასი: 442 გპა | |||||||||||||||||||||||||||
| პუასონის კოეფიციენტი | ალმასი: 0.1 | |||||||||||||||||||||||||||
| მოოსის მეთოდი |
გრაფიტი: 1–2 ალმასი: 10 | |||||||||||||||||||||||||||
| CAS ნომერი |
7440-44-0 7782-42-5 7782-40-3 | |||||||||||||||||||||||||||
| ისტორია | ||||||||||||||||||||||||||||
| აღმომჩენია | ეგვიპტელებმა და შუმერებმა (ძვ. წ. 3750) | |||||||||||||||||||||||||||
| პირველი მიმღებია | ანტუან ლავუაზიე (1789) | |||||||||||||||||||||||||||
| ნახშირბადის მთავარი იზოტოპები | ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
| • | ||||||||||||||||||||||||||||
ნახშირბადი[1][2] (ლათ. Carboneum < ლათ. carbō — „ნახშირი“; ქიმიური სიმბოლო — ) — ელემენტთა პერიოდული სისტემის მეორე პერიოდის, მეთოთხმეტე ჯგუფის (მოძველებული კლასიფიკაციით — მეოთხე ჯგუფის მთავარი ქვეჯგუფის, IVა) ქიმიური ელემენტი. მისი ატომური ნომერია 6, ატომური მასა — 12.011; სიმკვრივე (თხევად მდგომარეობაში) — 2.08 გ/სმ3; ბუნებრივი ნახშირბადი შედგება ორი სტაბილური იზოტოპისაგან: (98.892 %) და (1.108 %). რადიოაქტიური იზოტოპებიდან ყველაზე მნიშვენლოვანია (T1/2=5.6×103 წ). ხელოვნური გზით მიღებულია ნახშირბადის არამდგრადი ნუკლიდები, რომელთა მასური რიცხვი მერყეობს 8-23-ის შუალედში.
ისტორია
[რედაქტირება | წყაროს რედაქტირება]ნახშირბადი ხის ნახშირის სახით გამოიყენებოდა ძველი დროიდან ლითონების გამოსადნობად. ძველთაგანვე ცნობილია ნახშირბადის ალოტროპიული მოდიფიკაცია — ალმასი და გრაფიტი. ნახშირბადის ელემენტარული ბუნება დადგენილია ანტუან ლავუაზიეს მიერ 1780-იან წლებში.
დასახელების წარმომავლობა
[რედაქტირება | წყაროს რედაქტირება]საერთაშორისო სახელწოდება მოდის ლათ. carbō «ნახშირი».
ფიზიკური თვისებები
[რედაქტირება | წყაროს რედაქტირება]ნახშირბადი არსებობს მრავალი ალოტროპული მოდიფიკაციას სახით სხვადასხვა ფიზიკური თვისებებით. მოდიფიკაციის სხვადასხვაობა განპიროვნებულია ნახშირბადის უნარით წარმოქმნას სხვადასხვა ტიპის ქიმიური კავშირები. ცნობილია ნახშირბადის ხუთი ალოტრპული მოდიფიკაცია - ალმასი, კარბინი, გრაფინი, გრაფიტი და ფულერენი. ალმასისა და გრაფიტის კრისტალური სტრუქტურა ატომურია, მაგრამ ისინი ერთმანეთისაგან განსხვავდებიან მესერში ატომების განლაგებით. ალმასის კრისტალურ მესერში ნახშირბადის თითოეული ატომი სხვა ატომებთან ახორციელებს ოთხ კოვალენტურ ბმას ტეტრაედრის წვეროების მიმართულებით (ბმის კუთხე - 109,28o, ბმის სიგრძე - 0,154 ნმ). ამით აიხსნება ალმასის დიდი სიგრძე. გრაფიტში ნახშირბადის ატომები განლაგებულია წესიერი ექსკუთხედის წვეროებში, რომლებიც შრეებს ქმნიან. მეზობელ პარალელურ შრეებს შორის მანძილი გაცილებით მეტია (0,335 ნმ), ვიდრე ერთსა და იმავე შრეში მეზობელ ატომებს შორის (0,142 ნმ). ეს იწვევს შრეებს შორის კავშირის შესუსტებას, რის გამო უბრალო მექანიკური ზემოქმედებითაც კი გრაფიტი ადვილად იშლება ფენებად, რომლებიც თავისთავად ძალიან მტკიცეა. ალმასის სიმკვრივე - 3510 კგ/მ3 , გრაფიტის სიმკვრივე - 2250 კგ/მ³, tლღ 3570oC, tდუღ 4200oC. ალმასი ელექტრულ დენსა და სითბოს არ ატარებს. გრაფიტს ახასიათებს ლითონური ბზინვა; ელექტრული დენისა და სითბოს კარგი გამტარია. ალმასი ყველა ბუნებრივ ნივთიერებაზე მაგარია, გრაფიტი კი ქაღალდზე სუსტი გახახნუებითაც კი იშლება და ტოვებს კვალს.
ალმასი და გრაფიტი მაღალ ტემპერატურაზე ურთიერთ გარდაიქმნება. გრაფიტი ალმასად გარდაიქმნება 2000oC, 100 000 ატმოსფერული წნევის პირობებში, ხოლო ალმასი გრაფიტის სახეს იღებს უჰაეროდ გახურების დროს - 1500oC.
ნახშირბადის მესამე მოდიფიკაცია - კარბინი ჰექსაგონალური სტრუქტურის შავი ფერის ფხვნილია. პირველად მიიღეს სინთეზის გზით, შემდეგ აღმოაჩინეს ბუნებაშიც. გახურების დროს (2800oC) გარდაიქმნება გრაფიტად.
უკანასკნელ პერიოდში აღმოაჩინეს ნახშირბადის კიდევ ორი მოდიფიკაცია - ფულერენი და გრაფინი.
ნახშირბადის იზოტოპები
[რედაქტირება | წყაროს რედაქტირება]ბუნებრივი ნახშირბადი შედგება ორი სტაბილური იზოტოპისაგან — 12С (98,93 %) და 13С (1,07 %) და ერთი რადიოაქტიური იზოტოპისაგან 14С (β-გამოსხივება, Т½= 5700 წ.), თავმოყრილია ატმოსფეროში და დედამიწის ქერქის ზედაპირზე. ის ყოველთვის იქმება სტრატოსფეროს ქვედა ფენებში კოსმიური გამოსხივების ნეიტრონების ზემოქმედების შედეგად აზოტის ბირთვებზე, შემდეგი რეაქციით: 14N (n, p) 14C, ასევე, 1950 წ., როგორც ატომური ელექტროსადგურის მუშაობის ტექნოგენური პროდუქტი და წყალბადის ბომბის გამოცდის შედეგი.
წარმოქმნაზე და დაშლაზე 14С დაფუძნებულია რადიონახშირბადული დატირების მეთოდი, ფართოდ გამოიყენება მეოთხედული გეოლოგიაში და არქეოლოგიაში.
ნახშირბადის ალოტროპიული მოდიფიკაცია
[რედაქტირება | წყაროს რედაქტირება]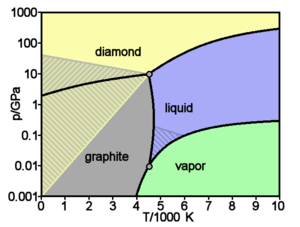
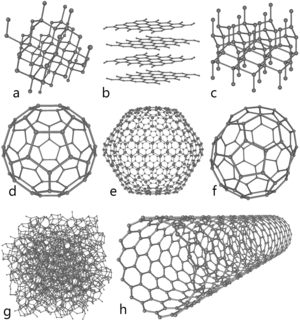
a: ალმასი, b: გრაფიტი, c: ლონსდეილიტი
d: ფულერენი — ბუკიბოლი C60, e: ფულერენი C540, f: ფულერენი C70
g: ამორფული ნახშირბადი, h: ნახშირბადის ნანომილაკი
- გრაფიტი
- ალმასი
- ცარბინი
- ლონსდეილიტი
- ფულერენი
- ნახშირბადის ნანომილაკები
- გრაფენი
- ამორფული ნახშირბადი
ნახშირბადის ატომის ელექტრონულ ორბიტალს შეიძლება ჰქონდეს სხვადასხვანაირი გეომეტრია, მისი ელექტრონული ორბიტალების ჰიბრიდიზაციის მიხედვით. არსებობს ნახშირბადის ატომის სამი ძირითადი გეომეტრია.
- ტეტრაედრული, წარმოიქმნება ერთი s- და სამი p- ელექტრონების შერევით (sp3-ჰიბრიდიზაცია). ნახშირბადის ატომი მდებარეობა ტეტრაედრის ცენტრში, შეკავშირებულია ოთხი ეკვივალენტური σ-კავშირით ნახშირბადის ატომთან ან სხათი ტეტრაედრის წვერთან. ნახშირბადის ატომის ასეთ გეომეტრიას შეესაბამება ნახშირბადის ალოტროპიული მოდიფიკაცია ალმასი და ლონსდეილიტი. ასეთი ჰიბრიდიზაციას ფლობს ნახშირბადი, მაგალითად, მეთანში და სხვა ნახშირწყალბადებში.
- ტრიგონალური, წარმოიქმნება ერთი s- და ორი p-ელექტრონული ორბიტალების შერევით (sp2-ჰიბრიდიზაცია). ნახშირბადის ატომს აქვს სამი თანაბარფასოვანი σ-კავშირი, რომლებიც განლაგებულნი არიან ერთ სიბრტყეზე 120° კუთხის დახრით ერთმანეთთან. ჰიბრიდიზაციაში არ მონაწილეობს p- ორბიტალი, რომელიც მდებარეობს σ-კავშირის სიბრტყის პერპენდიკულარულად, გამოიყენება π-კავშირის წარმოსაქმნელად სხვა ატომებთან. ნახშირბადის ასეთი გეომეტრია დამახასიათებელია გრაფიტისათვის, ფენილისათვის და სხვა.
- დიგონალური, წარმოიქმნება ერთი s- და ერთი p-ელექტრინის შერევით (sp-ჰიბრიდიზაცია). ამასთან ორი ელექტრონის ორბ. გაჭიმულია ერთი მიმართულებით და აქვს არასიმეტრიული ჰანტელის სახე. სხვა ორი р-ელექტრონი იძლევა π-კავშირს. ასეთი გეომეტრიის ატომის ნახშირბადი წარმოქმნის განსხვავებულ ალოტროპიულ მოდიფიკაციას — კარბინს.
2010 წ. ნოტინგემის უნივერსიტეტის თანამშრომლებმა სტივენ ლიდლმა და კოლეგებმა მიიღეს ნაერთი (მონომერული დილიტიო მეტანდი), სადაც ნახშირბადის ატომის ოთხი კავშირი მდებარეობენ ერთ სიბრტყეზე[3]. ადრე "ბრტყელი ნახშირბადის" შესაძლებლობა იწინასწარმეტყველა პაულ ფონ შლეიერის მიერ , მაგრამ ის არ იქნა სინთეზირებული.
გრაფიტი და ალმასი
[რედაქტირება | წყაროს რედაქტირება]ნახშირბადის ძირითადი და კარგად შესწავლილი ალოტროპიული მოდიფიკაციებია - ალმასი და გრაფიტი. ნორმალურ პირობებში თერმოდინამიკულად მდგრადია მხოლოდ გრაფიტი, ხოლო ალმასს და ნახშირბადის სხვა ფორმებს მეტასტაბილურნი არიან. ატმოსფერული წნევის და 1200 K მაღალი ტემპერატურისას ალმასი გადადის გრაფიტში, 2100 K ზევით კი გარდაქმნა ხდება მომენტალურად. ΔН0 გადასვლა — 1,898 კჯლ/მოლი. ნორმალური წნევისა და 3780 K ტემპერატურისას ნახშირბადი სუბლიმირდება. თხევადი ნახშირბადი არსებობს მხოლოდ გარკვეული გარე წნევის დროს. სამმაგი წერტილები: გრაფიტი-სითხე-ორთქლი Т = 4130 K, р = 10,7 მპა. გრაფიტის პირდაპირი გადასვლა ალმასში მიმდინარეობს 3000 K ტემპერატურისა და 11—12 გპა - წნევისას.
60 გ პა-ზე მეტი წნევისას სავარაუდოა უფრო მკვრივი, მჭიდრო მოდიფიკაციის წარმოქმნა С III (სიმკვრივე 15—20 %-ით უფრო მაღალია ვიდრე ალმასის), რომელსაც გააჩნია ლითონური გამტარობა. მაღალი წნევებისას და შედარებით დაბალი ტემპერატურებისას (მიახლ. 1200 K) მაღალორიენტირებული გრაფიტიდან წარმოიქმნება ნახშირბადის ჰექსაგონალური კრისტალური მესერიანი მოდიფიკაცია, ვიურციტის ტიპის — ლონდსდეილიტი (а = 0,252 ნმ, с = 0,412 ნმ, სივრცებრივი ჯგუფი Р63/mmc), სიმკვრივე 3,51 გ/სმ³, ანუ ისეთივე, როგორც ალმასი. ლონსდეილიტი ნაპოვნია ასევე მეტეორიტებში.
ულტრადისპერსიული ალმასები (ნანოალმასი)
[რედაქტირება | წყაროს რედაქტირება]1980 წ. სსრკ-ში იქნა აღმოჩენილი ის, რომ ნახშირბადშემცველი მასალების დინამიკური დატვირთვის პირობებში შესაძლებელი წარმოიქმნეს ალმასის მსგავსი სტრუქტურები, რომლებმაც მიიღო ულტრადისპერსიული ალმასის სახელწოდება (უდა). თანამედროვე დროს ხშირად იხმარება ტერმინი «ნანოალმასი». ასეთი მასალებში ნაწილაკების ზომები შეადგენს ნანომეტრის ერთეულებს. უდა-ს წარმოქმნის პირობები შეიძლება რეალიზებულ იქნას ასაფეთქებელი ნივთიერებების დეტონაციის დროს მნიშვნელოვანი უარყოფითი ჟანგბადის ბალანსით, ტროტილისა და ჰექსოგენის ნარევის მაგალითზე. ასეთი პირობები შეიძლება რეალიზებულ იქნას ციური სხეულების დედამიწასთან შეჯახების დროს ნახშირბადშემცველი მასალების (ორგანიკა ტორფი, ნახშირი და სხვა) თანხლებით. ასე რომ ტუნგუსკის მეტეორიტის ვარდნის ზონაში ტყიან საგებელში აღმოჩენილ იქნა - უდა.
კარბინი
[რედაქტირება | წყაროს რედაქტირება]ნახშირბადის ჰექსაგონალური სინგონიის კრისტალურ მოდიფიკაციას მოლეკულების ჯაჭვური აღნაგობით ეწოდება კარბინი. ჯაჭვებს აქვს ან პოლიენური (—C≡C—), ან პოლიკუმულენური (=C=C=) აღნაგობა. ცნობილია კარბინის რამდენიმე ფორმა, რომლებიც განსხვავდებიან ელემენტარული უჯრედში ატომების რაოდენობით, უჯრედების ზომები და სიმკვრივე (2,68—3,30 გ/სმ³). ბუნებაში კარბინი გვხვდება მინერალ ჩაოიტის სახით (თეთრი ძარღვები და ჩანართები გრაფიტში) და მიღებულია ხელოვნურადაც - აცეტილენის მჟანგავი დეჰიდროპოლიკონდენსაციით, გრაფიტზე ლაზერული დასხივებით, ნახშირწყალბადებში ან CCl4 დაბალტემპერატურული პლაზმაში.
კარბინი წარმოადგენს მწვრილკრისტალური შავი ფერის ფხვნილს (სიმკვრივე 1,9-2 გ/სმ³), გააჩნია ნახევარგამტარების თვისებები. მიღებულია ხელოვნურად ნახშირბადის გრძელი ატომების ჯაჭვებისაგან, განლაგებული არიან პარალელურად ერთმანეთთან.
კარბინი — ნახშირბადის სიგძივი პოლიმერია. კარბინის მოლეკულაში ნახშირბადის ატომები შეერთებულია ჯაჭვად რიგრიგობით ან სამმაგი და ერთმაგი კავშირით (პოლიენური აღნაგობა), ან მუდმივი ორმაგი კავშირებით (პოლიკუმულებური აღნაგობა). ეს ნივთიერება პირველად მიგებული იქნა საბჭოთა ქიმიკოსების ვ. ვ. კორშაკის, ა. მ. სლადკოვის, ვ. ი. კასატოჩკინის და ი. პ. კუდრიავცევის მიერ 60-წლებში. ელემენტოორგანული ნაერთების ინსტიტუტში[4]. კარბინს ახასიათებს ნახევარგამტარის თვისებები, ამასთან სინათლის ზემოქმედებით მისი გამტარობა ძლიერ იზრდება. ამ თვისებაზეა დაფუძნებული მისი პირველი პრაქტიკული გამოყენება - ფოტოელემენტებში.
ნახშირბადი ცნობილია ასევე კლასტერული ნაწილაკების სახით С60, С70, C80, C90, C100 და მსგავსი (ფულერენი), ასევე გრაფენების, ნანომილაკები და რთული სტრუქტურებიანი — ასტრალენი.
ამორფული ნახშირბადი
[რედაქტირება | წყაროს რედაქტირება]ამორფული ნახშირბადის აღნაგობის საფუძვლია მონოკრისტალური (ყოველთვის შეიცავს მინარევებს) გრაფიტი. ეს არის ქვანახშირის კოქსი, მურა და ქვანახშირი, ტექნახშირბადი, მური, აქტიური ნახშირი.
გრაფენი
[რედაქტირება | წყაროს რედაქტირება]გრაფენი (англ. graphene) — ნახშირბადის ორგანზომილიანი ალოტროპიულ მოდიფიკაციას წარმოადგენს, რომელიც წარმოიქმნება ერთი ატომის სისქის ფენით, ნაერთი sp² კავშირის მეშვეობით, ჰექსაგონალური ორგანზომილებიანი კრისტალური მესერით.
ბუნებაში არსებობა
[რედაქტირება | წყაროს რედაქტირება]ნახშირბადის შემცველობა დედამიწის ქერქში მასის 0,1 %-ია. თავისუფალი ნახშირბადი ბუნებაში ალმასისა და გრაფიტის სახით გვხვდება. ნახშირბადის ძირითადი მასა ბუნებრივი კარბონატების (კირქვები და დოლომიტები), საწვავი წიაღისეულის - ანტრაციტი (94—97 % С), მურა ნახშირის (64—80 % С), ქვანახშირის (76—95 % С), საწვავი შრეების (56—78 % С), ნავთობის (82—87 % С), საწვავი ბუნებრივი აირის (99 %-მდე მეთანი), ტორფების (53—56 % С), ასევე ბიტუმის და სხვა სახით გვხვდება. ნახშირბადი დედამიწის ატმოსფეროში და ჰიდროსფეროში არსებობს ნახშირორჟანგის სახით СО2, ჰაერში მასის 0,046 % СО2, მდინარეების, ზღვებისა და ოკეანეების წყლებში ~60 -ჯერ მეტია. ნახშირბადი შედის მცენარეებისა და ცხოველების შემადგენლობაში(~18 %).
ადამიანის ორგანიზმში ნახშირბადი ხვდება საკვებთან ერთად (ნორმაა მიახლოებით 300 გ დღეღამეში). ნახშირბადის საერთო შემცველობა ადამიანის ორგანიზმში აღწევს მიახლოებით 21 % (15 კგ - 70 კგ სხეულის წონაზე). ნახშირბადი შეადგენს კუნთების მასის 2/3 ნაწილს და ძვლების მასის 1/3 ნაწილს. ორგანიზმიდან გამოდის უპირატესად ჰაერის ამოსუნთქვასთან ერთად (ნახშირორჟანგი) და შარდთან ერთად.
ნახშირბადის მიმოქცევა ბუნებაში ჩართულია ბიოლოგიურ ციკლში, СО2-ის გამოყოფა ატმოსფეროში წიაღისეული საწვავის წვის დროს, ვულკანური აირებიდან, ცხელი მინერალური წყაროებიდან, ოკეანის წყლების ზედა ფენებიდან და სხვა. ბიოლოგიური ციკლი შემდეგში მდგონარეობს, ნახშირბადი СО2 სახით ტროფოსფეროდან შთაინთქმება მცენარეების მიერ. შემდეგ ბიოსფეროდან ხელახლა ბრუნდება გეოსფეროში: მცენარეებთან ერთად ნახშირბადი ხვდება ცხოველებისა და ადამიანის ორგანიზმში, შემდეგ კი ცხოველებისა და მცენარეების ლპობის შედეგად - ნიადაგში და СО2 სახით — ატმოსფეროში.
ორთქლისმაგვარ მდგომარეობაში აზოტთან და წყალბადთან ნაერთების სახით ნახშირბადი აღმოჩენილია მზის ატმოსფეროში, პლანეტებზე, ქვის და რკინის მეტეორიტებზე.
ნახშირბადის უმეტესი შენაერთი, და უპირველყოვლისა ნახშირწყალბადები, ხასიათდებიან გამოკვეთილი კოვალენტური კავშირებით. ჩვეულებრივი, ორმაგი და სამმაგი ატომების კავშირების სიმტკიცე ერთმანეთთან, მდგრადი ჯაჭვების წარმოქმნის შესაძლებლობები და ატომების ციკლი განაპირობებს ნახშირბადშემცველი ნაერთების უდიდესი რაოდენობის არსებობას, რომელსაც შეისწავლის ორგანული ქიმია.
ქიმიური თვისებები
[რედაქტირება | წყაროს რედაქტირება]ჩვეულებრივი ტემპერატურის პირობებში ნახშირბადი ქიმიურად ინერტულია, საკმაოდ მაღალი ტემპერატურის დროს კი უერთდება ბევრ ელემენტს, ავლენს ძლიერ აღმდგენ თვისებებს. სხვადასხვა ფორმის ნახშირბადის ქიმიური აქტივობა მცირდება რიგის მიხედვით: ამორფული ნახშირბადი, გრაფიტი, ალმასი, ჰაერზე ისინი აალდებიან შესაბამისად უფრო მაღალ ტემპერატუერაზე ვიდრე 300—500 °C, 600—700 °C და 850—1000 °C.
დაჟანგვის ხარისხი +4, −4, იშვიათად +2 (СО, ლითონების კარბიდები), +3 (C2N2, ჰალოგენციანები); იონიზაციის ენერგია თანმიმდევრობითი გადასვლით С0 დან С4+-მდე შესაბამისად 11,2604, 24,383, 47,871 და 64,19 ევ.
არაორგანული შენაერთები
[რედაქტირება | წყაროს რედაქტირება]ნახშირბადი რეაგირებს ბევრ ელემენტთან. ნაერთებს არალითონებთან აქვს თავისი სახელწოდება — მეთანი, ტეტრაფტორმეთანი.
ნახშირბადის ჟანგბადში წვის პროდუქტებია CO და CO2 (ნახშირბადის მონოქსიდი და ნახშირბადის დიოქსიდი შესაბამისად). ცნობილია ასევე არამდგრადი ოქსიდი С3О2 (დნობის ტემპერატურა −111 °C, დუღილის ტემპერატურა 7 °C) და სხვა ზოგი ოქსიდი. გრაფიტი და ამორფული ნახშირბადი იწყებს რეაგირებას წყალბადთან ტემპერატურაზე 1200 °C, ფთორთან 900 °C-ის დროს.
ნახშირორჟანგი (ნახშირბადის დიოქსიდი) რეაგირებს წყალთან, რომელიც წარმოქმნის სუსტ ნახშირმჟავას — H2CO3, რომლებიც წარმოქმნიათ მარილებს — კარბონატებს. დედამიწაზე ფართოდაა გავრცელებული კარბონატები: კალციუმის კარბონატი (მინერალური ფორმებია — ცარცი, მარმარილო, კალციტი, კირქვა და სხვა) და მაგნიუმის კარბონატი (მინერალური ფორმაა დოლომიტი).
გრაფიტი ჰალოგენებთან, ტუტე ლითონებთან და სხვა. ნივთიერებთან წარმოქმნიან კლატრატებს. ელექტრო მუხტის გატარებისას ნახშირის ელექტროდებს შორის აზოტის ატმოსფეროში წარმოიქმნება ციანი. მაღალი ტემპერატურების დროს ნახშირბადის ურთიერთქმედებით Н2 და N2 ნარევებთან მიიღებენ სინილის მჟავას (ციანის მჟავა): ნახშირბადის გოგირდთან ურთიერთქმედებისას წარმოიქმნება გოგირდნახშირბადი CS2, ცნობილია ასევე CS და C3S2. ლითონების უმრავლებოსთან, ბორთან და სილიციუმთან ნახშირბადი ქმნის კარბიდებს, მაგალითად:
მრეწველობისთვის მნიშვნელოვანია ნახშირბადისა და წყლის ორთქლის რეაქცია:
- (იხ. მყარი საწვავების გაზიფიკაცია).
გახურებისას ნახშირბადი აღადგენს ლითონებს ლითონების ოქსიდებიდან. ეს თვისება ფართოდ გამოიყენება მეტალურგიულ მრეწველობაში.
ორგანული ნაერთები
[რედაქტირება | წყაროს რედაქტირება]ნახშირბადის თვისების გამო - წარმოქმნას პოლიმერული ჯაჭვები, არსებობს ნახშირბადის საფუძველზე ნაერთების დიდი კლასი, რომლებიც მნიშვნელოვნად ბევრია, ვიდრე არაორგანული ნაერთები, და რომლებსაც შეისწავლის ორგანული ქიმია. მათ შორის ყველაზე ფართო ჯგუფებია: ნახშირწყალბადები, ცილები, ცხიმები და სხვა.
ნახშირბადის ნაერთები შეადგენენ დედამიწის სიცოცხლის საფუძველს, ხოლო მათი თვისება განსაზღვრავს პირობების სპექტრს, სადაც მსგავს სიცოცხლის ფორმებს შეუძლიათ არსებობა. ცოცხალ უჯრედებში ატომების რაოდენობის მიხედვით ნახშირბადი შეადგენს მიახლოებით 25 %, მასური წილის მიხედვით - მიახლოებით 18 %.
გამოყენება
[რედაქტირება | წყაროს რედაქტირება]გრაფიტი გამოიყენება ფანქრების წარმოებაში. ასევე მას იყენებენ საპოხ მასალას განსაკუთრებულად მაღალ ან დაბალ ტემპერატურებზე.
ალმასი, განსაკუთრებული სიმაგრის გამო, შეუცვლელლია როგორც აბრაზიული მასალა. ალმაზის დეპონირება აქვს ბორმანქანებს. ამას გარდა, დაწახნაგებული, დამუშავებული ალმასი — ბრილიანტი გამოიყენება როგორც ძვირფასი ქვა ოქრომჭედლობაში. თავისი იშვიათობის, მაღალი დეკორატიული თვისებების და ისტორიული გარემოებების გამო, ბრილიანტი უცვლელად წარმოადგენს ყველაზე ძვირადღირებულ ძვირფას ქვას.
ალმასის განსაკუთრებულად მაღალი თბოგამტარობის გამო (2000 ვტ/მ·К) ის ხდება პერსპექტიულ მასალად ნახევარგამტარულ თექნიკაში ცენტრალური პროცესორის საფენად. მაგრამ შედარებით მაღალი ფასი (მიახლოებით 50 დოლ/გრ) და დამუშავების სირთულე ზღუდავს მის გამოყენებას ამ დარგში.
ფარმაკოლოგიაში და მედიცინაში ფართოდ გამოიყენება ნახშირბადის სხვადასხვაგვარი ნაერთები — ნახშირმჟავას და კარბონის მაჟავის წარმოებულები, სხვადასხვანაირი ჰეტეროციკლები, პოლიმერები და სხვა ნაერთები. კარბოლენი (აქტივირებული ნახშირი), გამოიყენება ორგანიზმიდან სხვადასხვა ტოქსინების აბსორბაციისათვის და მათი გამოყვანისათვის გარეთ; გრაფიტი (მალამოების სახით) — კანის დაავადებების სამკურნალოდ; რადიოაქტიული ნახშირბადის იზოტოპები — მეცნიერული კვლევებისათვის (რადიონახშირბადული ანალიზი).
ნახშირბადი თამაშობს უდიდეს როლს ადამიანის ცხოვრებაში. მისი გამოყენება ისეთივე მრავალფეროვანია, როგორც ამ ელემენტის მრავალსხაეობა.
ნახშირბადი წარმოადგენს ყველა ცოცხალი ორგანიზმის საფუძველს. ყველა ცოცხალი ორგანიზმი მნიშვნელოვანწილად შედგება ნახშირბადისაგან. ნახშირბადი - სიცოცხლის საფუძველია. ნახშირბადის წყაროს ცოცხალი ორგანიზმებისათვის წარმოადგენს ჩვეულებრივ СО2 ატმოსფეროდან და წყლიდან. ფოტოსინთეზის შედეგად ის ხვდება კვების ბიოლოგიურ ჯაჭვში, სადაც ცოცხალი არსებები ჭამენ ერთმანეთს ან ერთმანეთის ნაშთს, რის შედეგაც მოიპოვებენ ნახშირბადს თავისი სხეულის განსავითარებლად. ნახშირბადის ბიოლოგიური ციკლი მთავრდება ან ჟანგვით და ატმოსფეროში დაბრუნებით ან წიაღისეულ შრეებად ნახშრისა და ნავთობის სახით.
ნახშირბადი წიაღისეული საწვავის სახით არის: ქვანახშირი და ნახშირწყალბადები (ნავთობი, ბუნებრივი აირი) — ერთ-ერთი მთავარი მნიშვნელოვანი ენერგიის წყარო ადამიანისათვის.
ტოქსიკური მოქმედება
[რედაქტირება | წყაროს რედაქტირება]ნახშირბადი შედის ატმოსფერული აეროზოლების შემადგენლობაში, რის შედეგად შეიძლება შეცვალოს რეგიონალური კლიმატი, შემცირდეს მზიანი დღეების რაოდენობა. ნახშირბადი გარემოში ხვდება: მურის სახით ავტომანქანების გამონაბოლქვის შემადგენლობაში, ნახშირის წვის დროს თბოელექტროსადგურებში, ნახშირის ღია მოპოვებისას, მისი მიწისქვეშა გაზიფიკაციისას, ნახშირის კონცენტრატების მიღებისას და სხვა. ნახშირბადის კონცენტრაცია წვის წყაროს ზემოთ არის 100—400 მკგ/მ³, მსხვილ ქალაქებში 2,4—15,9 მკგ/მ³, სოფლის რაიონებში 0,5 — 0,8 მკგ/მ³. ატომური ელ. სადგურების აეროზოლური გამონაბოლქვით ატმოსფეროში ხვდება (6—15)×109 ბკ/დღეღამე 14СО2.
ნახშირბადის მაღალი შემცველობა ატმოსფერულ აეროზოლებში იწვევს მოსახლეობის დაავადების ზრდას, განსაკუთრებულად ზედა სასუნთქი გზების და ფიტვების. პროფესიული დაავადებები — ძირითადად ანტრაკოზი და ბრონქიტი. სამუშაო ზონის ჰაერში, მგ/მ³: ალმასი 8,0, ანტრაციტი და კოქსი 6,0, ქვანახშირი 10,0, ტექნიკური ნახშირბადი და ნახშიბადიანი მტვერი 4,0; ათმოსფერულ ჰაერში ერთჯერადად მაქსიმალური 0,15, საშუალო დღეღამური 0,05 მგ/მ³.
ტოქსიკური მოქმედება 14С, ცილების მოლეკულების შემადგენლობაში (განსაკუთრებულად დნმ), განისაზღვრება მსი რადიაციული ურთიერთქმედებით β-ნაწილაკებთან (14С (β) → 14N), რომელიც იწვევს ცვლილებებს მოლეკულის ქიმიურ შემადგენლობაში. დასაშვები კონცენტრაცია 14С სამუშაო ზონის ჰაერში არის А 1,3 ბკ/ლ, ატმოსფერულ ჰაერში Б 4,4 ბკ/ლ, წყალში 3,0×104 ბკ/ლ, ზღვრული დასაშვები ნორმა სასუნთქი ორგანოებიდან 3,2×108 ბკ/წელი.
იხილეთ აგრეთვე
[რედაქტირება | წყაროს რედაქტირება]ლიტერატურა
[რედაქტირება | წყაროს რედაქტირება]- ჰიპერკოორდინირებული ნახშირბადის ქიმია, თარგმნ. ინგლ., მ., 1990.
- Kirk — Othmer encyclopedia, 3 ed., vol.4, N.-Y., 1978, p. 556-709.
- ბუნებრივი ენერგომატარებლების და ნახშირბადული მასალების ქიმია დაარქივებული 2005-09-20 საიტზე Wayback Machine. ტ. ვ. ბიხარკინა, ნ. გ. დიგუროვი
- В.І. Саранчук, В. В. Ошовський, Г. О. Власов. Хімія і фізика горючих копалин . — Донецьк: Східний видавничий дім, 2003. ?204 с.
- სლადკოვი ა. მ., კუდრიავცევი ი. პ. ალმასი, გრაფიტი, კარბინი — ნახშირბადის ალოტროპიული ფორმები // პრიროდა. 1969.№ 5. С.37-44.
რესურსები ინტერნეტში
[რედაქტირება | წყაროს რედაქტირება]- ნახშირბადი Webelements-ზე
- ნახშირბადი ქიმიური ელემენტების პოპულარულ ბიბლიოთეკაში
- ინფორმაცია ნახშირბადზე დაარქივებული 2011-01-21 საიტზე Wayback Machine.
- ალექსეი სლადკოვის ნახშირბადი — კარბინის აღმოჩენის ისტორია
- სლადკოვი კარბინი — ნახშირბადის მესამე ალოტროპილი ფორმა: მონოგრაფია
სქოლიო
[რედაქტირება | წყაროს რედაქტირება]- ↑ დოლიძე ვ., ციციშვილი ვ., „ოთხენოვანი ქიმიური ლექსიკონი“, თბ., 2004, გვ. 226
- ↑ ქართული საბჭოთა ენციკლოპედია, ტ. 7, თბ., 1984. — გვ. 355.
- ↑ ა. ბორისოვა. (30.07.2010) ქიმიკოსებმა გააბრტყელეს ნახშირბადი. Gazeta.ru. ციტირების თარიღი: 2010-08-22.
- ↑ V. I. Kasatochkin, A. M. Sladkov, et al., Dokl. Akad. Nauk SSSR, 177, No. 2, 358 (1967)
| ქიმიურ ელემენტთა პერიოდული სისტემა | |||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |||||||||||
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||||||||||
| 8 | 119 | 120 | ⁂ | 143 | 144 | 145 | 146 | 147 | 148 | 149 | 150 | 151 | 152 | 153 | 154 | 155 | 156 | 157 | 158 | 159 | 160 | 161 | 162 | 163 | 164 | 165 | 166 | 167 | 168 | 169 | 170 | 171 | 172 | ||||||||||
| ⁂ | 121 | 122 | 123 | 124 | 125 | 126 | 127 | 128 | 129 | 130 | 131 | 132 | 133 | 134 | 135 | 136 | 137 | 138 | 139 | 140 | 141 | 142 | |||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||









