სითხე
სითხე — ნივთიერების ერთ-ერთი აგრეგატული მდგომარეობა. სითხის ძირითად თვისებას, რომლითაც ის განსხვავდება სხვა აგრეგატული მდგომარეობისაგან, წარმოადგენს თვისება განუსაზღვრელად შეიცვალოს ფორმა მექანიკური დაძაბულობა ზემოქმედებით, ძალიან მცირედიც კი, ამასთან პრაქტიკულად მოცულობის შენარჩუნებით.
თხევად მდგომარეობას ჩვეულებრივ მიიჩნევენ შუალედურ მდგომარეობად მყარ სხეულსა და აირს შორის: აირი არ ინარჩუნებს მოცულობას, ფორმას, ხოლო მყარი სხეული ინარჩუნებს ერთსაც და მეორესაც.
სითხის ფორმა შეიძლება მთლიანად ან ნაწილობრის განისაზღვრებოდეს იმით, რომ მისი ზედაპირი ისე მოქმედებს როგორც დრეკადი, ელასტიური მემბრანა. ასე წყალი შეიძლება შეიკრას წვეთად. მაგრამ სითხეს შეუძლია მიედინებოდეს საკუთარი უძრავი ზედაპირის ქვეშ, და ეს ასევე ნიშნავს ფორმის შეუნარჩუნებლობას (თხევადი სხეულის შიდა ნაწილების).

სითხის მოლეკულებს არ გააჩნიათ გარკვეული მდებარეობა, მაგრამ ამავე დროს გადაადგილების სრული თავისუფლებაც მიუწვდომელია. მათ შორის არის მიზიდულობა, საკმაოდ ძლიერი, რათა შეაკავონ ისინი ახლო მანძილზე.
ნივთიერება თხევად მდგომარეობაში ტემპერატურის გარკვეულ ინტერვალში არსებობს, რომლის ქვევით ის გადადის მყარ მდგომარეობაში (მიმდინარეობს კრისტალიზაცია ან გამაგრების ამორფულ მდგომარეობაში გადასვლა - მინა), მაღლა კი - აიროვან მდგომარეობაში გადადის (ხდება აორთქლება). ამ ინტერვალის საზღვრები დამოკიდებულია წნევაზე.
როგორც წესი, ნივთიერებას თხევად მდგომარეობაში აქვს მხოლოდ ერთი მოდიფიკაცია. (ყველაზე მნიშვნელოვანი გამონაკლისია - კვანტური სითხეები და თხევადი კრისტალები.) ამიტომ უმეტეს შემთხვევაში სითხე წარმოადგენს არა მარტო აგრეგატულ მდგომარეობას, არამედ თერმოდინამიკულ ფაზას (თხევადი ფაზა).
მიღებულია ყველა სითხის დაყოფა სუფთა სითხეებად და ნარევებად (ნაზავი). ზოგიერთ სითხის ნაზავს სიცოცხლისთვის აქვს დიდი მნიშვნელობა: სისხლი, ზღვის წყალი და სხვა. სითხეებს შეუძლიათ გამხსნელების ფუნქცია შეასრულოს.
ტექნიკურ ჰიდრომექანიკაში სითხეს უწოდებენ ფიზიკურ სხეულს, რომელიც ფლობს: ა) მყარი სხეულისაგან განსხვავებით დენადობას; და ბ) აირისაგან განსხვავებით თავისი მოცულობის ძალიან მცირე ცვლილებით. ზოგჯერ სითხეს მისი ფართო მნიშვნელობით აირსაც უწოდებენ; ამასთან სითხე სიტყვის ვიწრო გაგებით, რომელიც აკმაყოფილებს პირობებს ა) და ბ) უწოდებენ წვეთოვან სითხეს.
თხევადი ნაწილაკი — ეს არის სითხის ნაწილი, სიდიდით მცირე ვიდრე განსახილველი სითხის მოცულიბა, და ამასთან შეიცავს სითხის მოლეკულების მაკროსკოპიულ დიდ რაოდენობას.
სითხის ფიზიკური თვისებები[რედაქტირება | წყაროს რედაქტირება]
- დენადობა
სითხის ძირითად თვისებას ძარმოადგენს დენადობა. თუკი სითხის მონაკვეთთან, რომელიც წონასწორობაშია, მოვდებთ გარე ძალას, მაშინ წარმოიქმნება სითხის ნაწილაკების ნაკადი იმ მიმართულებით, საიდანაც ეს ძალაა მოდებული: სითხე მიედინება. ამიტომ, გაუწონასწორებელი გარე ძალების ზემოქმედებით სითხე ფორმას და შეფარდებითი ნაწიკაბეის მდებარეობას არ ინარჩუნებს და ამიტომაც იღებს ჭურჭლის ფორმას, რომელშიც ის იმყოფება.
პლასტიკური მყარი სხეულებისგან განსხვავებით, სითხეს არ გააჩნია დენადობის ზღვარი: საკმარისია როგორიც არ უნდა იყოს მცირე გარე ძალა მოდება, რათა სითხემ დინება დაიწყოს.
- მოცულობის შენარჩუნება
სითხის თვისებების ერთ-ერთ მახასიათებელს წარმოადგენს ის რომ მას აქვს გარკვეულ მოცულობა (გარე პირობებისას შეცვლის გარეშე). მექანიკურად სითხის შეკმშვა მეტისმეტად რთულია, რადგანაც აირებთან შედარებით, მოლეკულებს შორის თავისუფალი სივრცე ძალიან მცირეა. ჭურჭელში არსებულ სითხეზე მოქმედი წნევა უცვლელად და ერთნაირად გადაეცემა სითხის მოცულობის ყოველ წერტილს (პასკალის კანონი, მართებულია ასევევ აირებისათვის). ეს თავისებურება, სითხის მცირე კუმშვადობასთან ერთად, გამოიყენება ჰიდრავლიკურ მანქანებში.
სითხეები ჩვეულებრივ მოცულობაში იზრდებიან (ფართოვდებიან) გაცხელებისას და მცირდებიან მოცულობაში (იკუმშებიან) გაცივებისას. თუმცა გვხვდება გამონაკლისებიც, მაგალითად წყალი იკუმშება გახურებისას, ნორმალური წნევისა და ტემპერატურისას 0 °C-დან მიახლოებით 4 °C-მდე. ხოლო მაგალითად, ავტომობილების სამუხრუჭე სითხე, იკუმშება ძალიან ცუდად.
- სიბლანტე
ამას გარდა, სითხეები (როგორც აირეი) ხასიათდებიან სიბლანტით. ის განისაზღვრება როგორც უნარი გაუწიოს წინააღმდეგობა ერთი ნაწილის გადაადგილებას მეორის მიმართ - ანუ როგორც შიდა ხახუნი.
როდესაც სითხის მიმდებარე ფენები მოძრაობენ ერთმანეთის მიმართებაში, აუცილებლად ხდება მოლეკულების დამატებითი შეჯახებები ერთმანეთთან, იმ შეჯახებების გარდა რომელიც განპირობებულია სითბური მოძრაობით. აღიძვრება ძალები, რომლებიც ამუხრუჭებენ მოწესრიგებულ მოძრაობას. ამასთან მოწესრიგებული მოძრაობის კინეტიკური ენერგია გადადის სითბურში — მოლეკულების ქაოტური მოძრაობის ენერგიაში.
სითხე ჭურჭელში, მოყვანილი მოძრაობაში და მიშვებული თავის ნებაზე, თანდათანობით გაჩერდება, მაგრამ მისი ტემპერატურა აიწევს.

- თავისუფალი ზედაპირის წარმოქმნა და ზედაპირული დაჭიმულობა
მოცულობის შენარჩუნების გამო სითხეს შეუძლია თავისუფალი ზედაპირის შექმნა. ასეთი ზედაპირი წარმოადგენს ამ ნივთიერების ფაზის გაყოფის ზედაპირს: ერთ მხარეს მდებარეობს თხევადი ფაზა, მეორე მხარეს - აიროვანი ფაზა (ორთქლი), და, შეიძლება სხვა აირების იყოს მაგალითად, ჰაერი.
თუკი ერთი ნივთიერების თხევადი და აიროვანი ფაზები ერთმანეთს ეხებიან, წარმოიქმნება ძალები, რომლებიც მიისწრაფვიან გაყოფის ზედაპირის ფართობის შემცირებისაკენ — ეს არის ზედაპირის დაჭიმულობის ძალები. გაყოფის ზედაპირი მოქმედებს როგორც მემბრანა, რომელიც ცდილობს შეკუმშვას.
ზედაპირული დაჭიმულობა შეიძლება აიხსნას სითხის მოლეკულებს შორის არსებული მიზიდულობის ძალით. ყოველი მოლეკულა იზიდავს სხვა მოლეკულებს, ცდილობს «გარსშემოირტყას» ისინი, რაც ნიშნავს ზედაპირიდან წასვლას. შესაბამისად ზედაპირი მიისწრაფვის შემცირებისაკენ.
ამიტომაც საპნის ბუშტები და მცირე ბუშტები დუღილის დროს ცდილობენ მიიღონ სფეროს ფორმა: მოცემული მოცულობისას მინიმალურ ზედაპირს სფერო, ბურთი ფლობს. თული სითხეზე მოქმედებს მხოლოდ ზედაპირის დაჭიმულობის ძალები, ის აუცილებლად მიიღებს სფეროს ფორმას — მაგალითად, წყლის წვეთი უწონობაში.
- აორთქლება და კონდენსაცია
აორთქლება — ნივთიერების თანმიმდევრობითი გადასვლა თხევად მდგომარეობიდან გაზისებურ მდგომარეობაში ფაზაში (ორთქლი).
სითბური მოძრაობისას ზოგიერთი მოლეკულა ტოვებს სითხეს მისი ზედაპირიდან და გადადის ორთქლში. ამასთან მოლეკულების ნაწილი კი ბრუნდება უკან ორთქლიდან სითხეში. თუ კი სითხიდან მიდის უფრო მეტი მოლეკულა ორთქლში, ვიდრე ბრუნდება, მაშინ ადგილი აქვს აორთქლებას.
კონდენსაცია — უკუპროცესია, სადაც ნივთიერება გადადის გაზისებური მდგომარეობიდან თხევად ფაზაში. ამასთან ორთქლიდან სითხეში გადადის უფრო მეტი მოლეკულა ვიდრე სითხიდან ორთქლში.
აორთქლება და კონდენსაცია — არათანასწორი პროცესია, ისინი მიმდინარეობენ მანამ, სანამ არ დამყარდება ლოკალური წონასწორობა (თუ კი დამყარდება), ამასთან სითხე შეიძლება მთლიანად აორთქლდეს, ან მოვიდეს წონასწორობაში თავის ორთქლთან, როდესაც სითხიდან გამოდის იმდენივე მოლეკულა, რამდენიც ბრუნდება.
- დუღილი
დუღილი — სითხის შიგნით ორთქლწარმოქმნის პროცესია. საკარისი მაღალი ტემპერატურის დროს ორთქლის წნევა ხდება უფრო მაღალი ვიდრე სითხის შიდა წნევა, და იწყება ორთქლის ბუშტების წარმოქმნა, რომლებიც (დედამიწის მიზიდულობის პირობებში) ამოტივტივდება ზედაპირისაკენ.
- სისველე (დასველება)
სისველე, დასველება — ზედაპირული მოვლენაა, რომელიც ჩნდება სითხის მყარ სხეულთან კონტაქტისას ორთქლის არსებობის პირობებში, ანუ სამი ფაზის გაყოფის საზღვარზე.
დასველება ახასიათებს - სითხის «მიკრობას» ზედაპირზე და მასზე გავრცელებას, ჩამოდინებას (ან, პირუკუ, წყალს უკუაგდებს და არ ჩამოედინება). არჩევენ სამ შემთხვევას: დაუსველობას, შეზღუდულ სისველეს და სრული დასველება.
- შეზავებულობა
შეზავებულობა — არის სითხის უნარია გაიხსნან, გაზავდნენ ერთმანეთში. სითხეების შეზავების მაგალითია: წყლისა და ეთილენის სპირტის შეზავება, ხოლო შეუზავლობის გაუხსნელობის მაგალითია: წყალი და თხევადი ზეთი.
- დიფუზია
ჭურჭელში ორი შეზავებადი სითხის არსებობისას, სითხის მოლეკულები სითბური მოძრაობის შედეგად თანდათანობით იწყებენ გაყოფის ზედაპირის გადალახვას, ამის გამო სითხეები ნელ-ნელა ერთმანეთს ერევიან. ამ მოვლენას დიფუზიას უწოდებენ (ეს ასევე ხდება სხვადასხვა აგრეგატულ მდგომარეობაში მყოფ ნივთიერებებს შორისაც).
- გადახურება და გადაცივება
სითხე შეიძლება გახურებულ იქნას დუღილის ტემპერატურაზე მაღლა, დუღილის გარეშე. ამისათვის საჭიროა თანაბარი გაცხელება, ტემპერატურის მნიშვნელოვანი ცვლილებების გარეშე, მოცულობის საზღვრებში და მექანიკური შემოქმედების გარეშე, როგორიცაა ვიბრაცია. გადახურებულ სითხეში თუ ჩავაგდებთ რაიმეს, ის მყისვე დუღდება. გადახურებული წყალი შეიძლება იოლად მივიღოთ მიკროტალღურ ღუმელში.
გადაცივება — არის სითხის გაცივება გაყინვის ტემპერატურაზე ქვევით მყარ მდგომარეობაში გადასვლის გარეშე. როგორც გახურებისას, გადაცივებისათვის საჭიროა უვიბრაციობა და ტემპერატურის მუდმივბა.
- სიმკვრივის, სიმჭიდროვის ტალღები
თუმცა სითხის შეკუმშვა მეტად რთულია, მიუხედავად ამისა წნევის შეცვლისას იცვლება მისი მოცულობა და სიმკვრივეც. ეს მყისვე არ ხდება; თუ კი იკუმშება სითხის ერთი ნაწილი, მაშინ სხვა მონაკვეთზე ასეთი შეკუმშვა გადაეცემა მცირედი დაგვიანებით. ეს ნიშნავს რომ, სითხის შიგნით ვრცელდება დრეკადი ტალღა, უფრო კონკრეტულად სიმკვრივის ტალღები. სიმკვრივესთან ერთად იცვლება სხვა ფიზიკური სიდიდეები, მაგალითად, ტემპერატურა.
თუ კი ტალღის გავრცელებისას სიმვრივე იცვლება საკმაოდ სუსტად, ასეთ ტალღას უწოდებენ ბგერით ტალღას.
თუ კი სიმკვრივე იცვლება საკმაოდ ძლიერად, მაშინ ასეთ ტალღას უწოდებენ დარტყმითი ტალღაა. დარტყმითი ტალღა სხვა განტოლებებით გამოისახება.
სიმკვრივის ტალღები სითხეში წარმოადგენენ გრძივ ტალღებს, ანუ სიმკვრივე იცვლება გრძივად ტალღის გავრცელების მიმართულებით. განედური დრეკადი ტალღები სითხეში არ არის, ფორმის შეუნარჩუნებლობის გამო.
დრეკადი ტალღები სითხეში დროთა განმავლობაში ქრებიან, მათი ენერგია თანდათანობით გადადის თბოენერგიაში. ჩაქრობის მიზეზი - სიბლანტეა, «კლასიკური შთანთქმა», მოლეკულური რელაქსაცია და სხვა. ამასთან მუშაობს ე.წ. მეორე, ანუ მოცულობითი სიბლანტე — სიმკვრივის ცვლილებისას შიდა ხახუნი. დარტყმითი ტალღა დროთა განმავლობაში, ჩაქრობის შედეგად გადადის ბგერით ტალღაში.
დრეკადი ტალღები სითხეში განიცდიან ასევე არაერთგვაროვნულ გაბნევას, გაფანტვას რასაც იწვევს მოლეკულების ქაოტური სითბური მოძრაობა.

- ტალღები ზედაპირზე
თუ კი სითხის ზედეპირის მონაკვთს გადავაადგილებთ, გადავწევთ წონასწორობის მდგომარეობიდან, მაშინ დაბრუნებულ ძალთა ზემოქმედებით ზედაპირი იწყებს მოძრაობას უკან წონასწორობის მდგომარეობისაკენ. ეს მოძრაობა შემდეგ არჩერდება, არამედ გარდაიქმნება წონასწორობის მდგომარეობასთან ახლო რხევით მოძრაობებში და ვრცელდება სხვა მონაკვეთებზე. ასე წარმოიქმნება ტალღები წყლის ზედაპირზე.
თუ დაბრუნების ძალა - არის უპირატესად სიმძიმის ძალები, მაშინ ასეთ ძალებს უწოდებენ გრავიტაციულ ტალღებს (არ აგერიოთ გრვიტაციის ტალღებში). გრავიტაციული ტალღები წყალზე ყველგან შეიძლება ვიხილოთ.
თუ დაბრუნების ტალღა — არის უპირატესად ზედაპირის დაჭიმულობის ძალა, მაშინ ასეთ ტალღებს კაპილარული ტალღები ეწოდებათ.
თუ კი ეს ძალები შეპირისპირებულია, მაშინ ასეთ ტალღებს უწოდებენ კაპილარულ-გრავიტაციულს. ტალღები სითხის ზედაპირზე ქრებიან სიბლანტისა და სხვა ფაქტორების გამო.

- სხვა ფაზებთან თანაარსებობა
ფორმალურად რომ ვთქვათ, თხევადი ფაზის ამავე ნივთიერების სხვა ფაზებთან - აიროვანი და კრისტალური - გაწონასწორებული თანაარსებობისათვის საჭიროა გარკვეული პირობები. გარკვეულ წნევაზე საჭიროა გარკვეული ტემპერატურა. მით უმეტეს, ბუნებაში და ტექნიკაში ყველგან სითხე თანაარსებობს ორთქლთან ერთად, ან ასევე მყარ აგრეგატულ მდგომარეობაში - მაგალითად, წყალი წყლის ორთქლთან და ხშირად ყინულთან ერთად (თუკი ორთქლს ჩავთვლით ცალკე ფაზად ჰაერთან ერთად). ეს აიხსნება შემდეგი მიზეზებით.
— არაგაწონასწორებული მდგომარეობა. სითხის აორთქლებისათვის საჭიროა დრო, სანამ სითხე არ აორთქლდება მთლიანად, ის თანაარსებობს ორთქლთან ერთად. ბუნებაში სულ ხდება წყლის აორთქლება და ასევე უკუპროცესი - კონდენსაცია.
— ჩაკეტილი მოცულობა. დახურულ ჭურჭელში სითხე იწყებს აორთქლებას, მაგრამ რადგანაც მოცულობა შეზღუდულია, ორთქლის წნევა მატულობს. სითხე ხდება გაჯერებული ჯერ კიდევ მანამ, სანამ სითხე ბოლომდე აორთქლდებოდეს, ეს მაშინ თუ მისი რაოდენობა იყო საკმაოდ დიდი. გაჯერებულობის მიღწევის დროს, აორთქლებული სითხის რაოდენობა ტოლია კონდენსირებული სითხის რაოდენობის, სისტემა მოდის წონასწორობაში. ასე რომ, შეზღუდულ მოცულობაში, დგინდება პირობები იმისათვის რომ სითხემ და ორთქლმა გაწონასწორებულ მდგომაარეობაში თანაიარსებონ.
— მიწის გრავიტაციის პირობებში ატმოსფეროს არსებობა. სითხეზე მოქმედებს ატმოსფერული წნევა (ჰაერი და ორთქლი), მაშინ როცა ორთქლისთვის უნდა იქნეს გათვალისწინებული პრაქტიკულად მხოლოდ მისი პარციალური წნევა. ამიტომაც ფაზის დიაგრამაზე სითხეს და მის ზედაპირზე არსებულ ორთქლს შეესაბამება სხვადასხვა წერტილები, თხევადი ფაზის არსებობის რაიონში და გაზისებური ფაზის არსებობის რაიონში შესაბამისად. ეს აორთქლებას არ შლის, მაგრამ აორთქლებისათვის საჭიროა დრო, რომლის დროსაც ორივე ფაზა თანაარსებობს. ამ პირობის გარეშე სითხეები ადუღდებოდნენ და აორთქლდებოდნენ ძალიან სწრაფად.
თეორია[რედაქტირება | წყაროს რედაქტირება]
მექანიკა[რედაქტირება | წყაროს რედაქტირება]
სითხეების და აირების მოძრაობის და მექანიკური წონასწორობის შესწავლას და მათ ურთიერთქმედებას, ასევე ურთიერთქმედებას მყარ სხეულებთან ეძღვნება მექანიკის განყოფილება - ჰიდროაერომექანიკა (ხშირად ეწოდება ასევე ჰიდროდინამიკა). ჰიდროაერომექანიკა — არის მექანიკის უფრო ფართო დარგის ნაწილი, ერთიანი არემოს მექანიკა.
ჰიდრომექანიკა — არის ჰიდროაერომექანიკის განყოფილება, რადაც განიხილება შეუკუმშვადი სითხეები. რადგანაც სითხეების შეკუმშვა იმდენად მცირეა რომ შეიძლება მისი უგულვებელყოფა. კუმშვადი სითხეებისა და აირების შესწავლას ეძღვნება გაზის დინამიკა.
ჰიდრომექანიკა იყოფა ჰიდროსტატიკად - რაც შეისწავლის შეუკუმშვადი სითხეების წონასწორობას, და ჰიდროდინამიკად - რაც შეისწავლის სითხის მოძრაობას (ვიწრო გაგებით).
ელექტროგამტარი და მაგნიტური სითხეების მოძრაობას შეისწავლის მაგნიტური ჰიდროდინამიკა. გამოყენებითი პრობლემების მოსაგვარებლად გამოიყენება ჰიდრავლიკა.
ჰიდროსტატიკის ძირითადი კანონია — პასკალის კანონი.
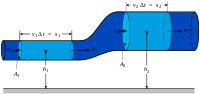
იდეალური უკუმშვადი სითხის მოძრაობას აღწერს ეილერის განტოლება. ასეთი სითხის სტაციონალური ნაკადისათვის სრულდება ბერნულის კანონი. ნახვრეტიდან სითხის გამოდინებას აღწერს ტორიჩელის ფორმულა.
ბლანტი სითხის მოძრაობას აღწერს ნავიე-სტოქსის განტოლება, სადაც შესაძლებელია შეკუმშვადობის გათვალისწინება.
სითხეებში (სხვა გარემოშიც) დრეკადი რხევები და ტალღები შეისწავლება აკუსტიკაში. ჰიდროაკუსტიკა - არის აკუსტიკის ნაწილი, სადაც რეალურ წყლის გარემოში შეისწავლება ბგერა , წყალქვეშა ლოკაციის და კავშირგაბმულობის მიზნით.
მოლეკულურ-კინეტიკური განხილვა[რედაქტირება | წყაროს რედაქტირება]
ნივთიერების აგრეგატული მდგომარეობა განისაზღვრება გარე პირობებით, ძირითადად წნევით და ტემპერატურით . მახასიათებელ პარამეტრებს წარმოადგენს მოლეკულის საშუალო კინეტიკური ენერგია და მოლეკულებს შორის ურთიერთქმედების საშუალო ენერგია (გათვლილი ერთ მოლეკულაზე) . სითხისათვის ეს ენერგიები მიახლოებით ტოლებია: მყარი სხეულებისათვის ურთიერთქმედების ენერგია კინეტიკურზე ბევრად მეტია, აირებისათვის - გაცილებით ნაკლები.
სითხეების კლასიფიკაცია[რედაქტირება | წყაროს რედაქტირება]
სითხის სტრუქტურა და ფიზიკური თვისებები დამოკიდებულია შემადგენელი ნაწილაკების ქიმიურ ინდივიდუალურობაზე და მათ შორის ურთიერთქმედების სიდიდეზე და ხასიათზე. შეიძლება გამოვყოთ სითხეების რამდენიმე ჯგუფი სირთულეების მატების მიხედვით.
1. ატომარული სითხეები ან ატომებისაგან შემდგარი სითხეები ან სფერული მოლეკულების სითხეები, დაკავშირებული ცენტრალური ვან დერ ვაალსის ძალებით (თხევადი არგონი, თხევადი მეთანი).
2. სითხეები ორ ატომიანი მოლეკულებით, შემდგარი ერთნაირი ატომებისაგან (თხევადი წყალბადი, თხევადი აზოტი). ასეთ მოლეკულებს ახასიათებთ კვადრუპოლური მომენტი.
3. თხევადი გარდაუვალი ლითონები (ნატრიუმი, ვერცხლისწყალი), სადაც ნაწილაკები (იონები) დაკავშირებულნი არიან შორსმპქმედი კულონის ძალებით.
4. სითხეები, შემდგარნი პოლარული მოლეკულებისაგან, რომლებიც დაკავშირებულნი არიან დიპოლ-დიპოლური ურთიერთქმედებით (თხევადი ბრომწყალბადი).
5. ასოცირებული სითხე, ან სითხეები წყალბადის კავშირით (წყალი, გლიცერინი).
6. სითხეები, შემდგარი დიდი მოლეკულებისაგან, რომელთათვის არსებითია შიდა თავისუფლების ხარისხი.
პირველი ორი ჯგუფის სითხეებს (ზოგჯერ სამის) ჩვეულებრივ უწოდებენ მარტივს. მარტივი სითხეები შესწავლილნი არიან უფრო კარგად ვიდრე სხები, არამარტივი (რთული) სითხეებიდან ყველაზე კარგად შესწავლილია წყალი. ამ კლასიფიკაციაში არ შედიან კვანტური სითხეები და თხევადი კრისტალები, რომლებიც წარმოადგენენ განსაკუთრებულ შემთხვევას და უნდა განიხილებოდეს ცალკე.
სტატისტიკური თეორია[რედაქტირება | წყაროს რედაქტირება]
ყველაზე წარმატებულად შეისწავლება სითხის სტრუქტურა და თერმოდინამიკური თვისებები პერკუს-იევეკის განტოლების დახმარებით.
თუ გამოვიყენებთ მყარი სფეროების მოდელს, ანუ თუ სითხის მოლეკულებს ჩავთვლით სფეროებად რომლის დიამეტრია , მაშინ პერკუს-იევიკის განტოლება შეიძლება ამოვხსნათ ანალიტიკურად და მივიღოთ სითხის მდგომარეობის განტოლება:
სადაც — ნაწილაკების რაოდენობა ერთეულ მოცულობაში, — უგანზომილებო სიმკვრივე. მცირე სიმკვრივეებისას ეს განტოლება გადადის იდეალური აირის მდგომარეობის განტოლება: . ზღვრული მაღალი სიმკვრივეებისას, , მიიღება არამკუნშვადი სითხეების მდგომარეობის განტოლება: .
მყარი სფეროების მოდელი არ ითვალისწინებს მოლეკულებს შორის მიზიდულობას, ამიტომ მასში არ არის მკვეთრი გადასვლები სითხესა და აირს შორის გარე პირობების ცვლილებისას.
თუ საჭიროა უფრო ზუსტი რეზულტატების მიღება, მაშინ სტრუქტურის და თვისებების ყველაზე კარგი აღწერა მიიღწევა გაღიზიანების თეორიით. ამ შემთხვევაში მყარი სფეროების მოდელი ითვლება ნულოვანი მიახლოებით, ხოლო მოლეკულებს შორის მიზიდულობის ძალა ითვლება გაღიზიანებად და იძლევიან შესწორებას.
კლასტერული თეორია[რედაქტირება | წყაროს რედაქტირება]
ერთ-ერთ თანამედროვე თეორიას წარმოადგენს «კლასტერული თეორია». მის საფუძლად არის იდეა, რომ სითხეს წარმოიდგენენ მყარი სხეულისა და აირის შეხამებას. ამასთან მყარი ფაზის ნაწილაკები (კრისტალები, რომლებიც მოძრაობენ მოკლე მანძილზე) განთავსდებიან ორთქლის ღრუბელში, სადაც ქმნის კლასტერულ სტრუქტურას. ნაწილაკების ენერგია პასუხობს ბოლცმანის განაწილებას, სისტემის საშუალო ენერგია ამასთან რჩება მუდმივი (მისი იზოლირებულობის პირობებში). ნელი ნაწილაკები ეჯახებიან კლასტერებს და ხდებიან მათი ნაწილი. ასე შეუსვენებლივ იცვლება კლასტერების კონფიგურაცია, სისტემა არის დინამიკური წონასწორობის მდგომარეობაში. სისტემაზე გარე ზემოქმედების შექმნისას სისტემა იმოქმედებს ლე შატელიე-ბრაუნის პრინციპით. ასე რომ, ადვილი ხდება ფაზური გარდაქმნების ახსნა:
- თანდათანობითი გაცხელებისას სისტემა თანდათანობით გარდაიქმნება აირად (დუღილი)
- გაცივებისას სისტემა თანდათანობით გარდაიქმნება მყარ სხეულად (გაყინვა).
იხილეთ აგრეთვე[რედაქტირება | წყაროს რედაქტირება]
რესურსები ინტერნეტში[რედაქტირება | წყაროს რედაქტირება]
| |||||||||||||||||













