გოგირდმჟავა
| გოგირდმჟავა | |
 | |
 | |
| ზოგადი | |
|---|---|
| სისტემური სახელწოდება | გოგირდმჟავა |
| ქიმიური ფორმულა | H2SO4 |
| ფარდ. მოლეკ. მასა | 98,082 მ. ა. ე. |
| მოლური მასა | 98,082 გ/მოლი |
| ფიზიკური თვისებები | |
| მდგომარეობა (სტ. პირ.) | სითხე |
| სიმკვრივე | 1,8356 გ/სმ³ |
| თერმული თვისებები | |
| დნობის ტემპერატურა | -10,38 °C |
| დუღილის ტემპერატურა | 279,6 °C |
| აალების ტემპერატურა | არ აალდება °C |
| დნობის კუთრი სითბო | 10,73 ჯ/კგ |
| ქიმიური თვისებები | |
| pKa | -3 |
| ხსნადობა წყალში | ირევა გ/100 მლ |
| ოპტიკური თვისებები | |
| გარდატეხის მაჩვენებელი | 1.397 |
| სტრუქტურა | |
| დიპოლური მომენტი | 2.72 დ |
| უსაფრთხოება | |
| LD50 | 510 |
| კლასიფიკაცია | |
| CAS | 7664-93-9 |
| RTECS | WS5600000 |
გოგირდმჟავა H2SO4 — ძლიერი ორფუძიანი მჟავა, რომელიც პასუხობს გოგირდის უმაღლეს დაჟანგვის ხარისხს (+6). ჩვეულებრივ პირობებში კონცენტრირებული გოგირდმჟავა - მძიმე ზეთისმაგვარი უფერო და უსუნო სითხეა. ტექნიკაში გოგირდმჟავას უწოდებენ როგორც მის წყლის ნარევსაც, ისე გოგირდის ანჰიდრიდთან SO3 ნარევსაც. თუ კი მოლური შეფარდება SO3 : H2O < 1, მაშინ ეს გოგირდმჟავის წყლახსნარია, თუ კი > 1 — SO3-ის ხსნარია გოგირდმჟავაში (ოლეუმი).
სახელწოდება
[რედაქტირება | წყაროს რედაქტირება]მე-XX საუკუნემდე გოგირდმჟავას ხშირად უწოდებდნენ შაბიამანს (როგორც წესი ეს იყო კრისტალური ჰიდრატი, რომელიც კონსისტენციით ზეთს ჩამოგავდა) ან შაბიაბნის ზეთს, ალბათ აქედანაა მისი მარილების სახელწოდებებიც (კერძოდ კი კრისტალ ჰიდრატების).
ფიზიკური და ფიზიკო-ქიმიური თვისებები
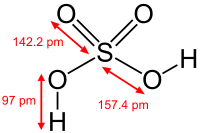
[რედაქტირება | წყაროს რედაქტირება]გოგირდმჟავა ძალიან ძლიერი მჟავაა, 18оС-ზე pKa (1) = −2,8, pKa (2) = 1,92 (К₂ 1,2 10−2); მოლეკულაში ბმების სიგრძეებია S=O 0,143 ნმ, S—OH 0,154 ნმ, კუთხე HOSOH 104°, OSO 119°; დუღილისას, წარმოქმნის აზოეტროპიულ ნარევს (98,3 % H2SO4 და 1,7 % H2О დუღილის ტემპერატურით 338,8оС). გოგირდმჟავა, რომელიც პასუხობს 100%-იან H2SO4 შემცველობას, აქვს შემდეგი შემადგენლობა (%): H2SO4 99,5, HSO4− — 0,18, H3SO4+ — 0,14, H3O+ — 0,09, H2S2O7, — 0,04, HS2O7⁻ — 0,05. წყალს შეერევა SO3-იც, ყველანაირი შეფარდებით. გოგირდმჟავა წყალხსნარებში პრაქტიკულად მთლიანად დისოცირდება H+, HSO4−, და SO₄2−. წარმოქმნის ჰიდრატებს H2SO4·nH2O, სადაც n = 1, 2, 3, 4 და 6,5.
ოლეუმი
[რედაქტირება | წყაროს რედაქტირება]გოგირდის ანჰიდრიდის SO3 ხსნარებს გოგირდმჟავაში უწოდებენ ოლეუმს, ისინი წარმოქმნიან ორ ნაერთს H2SO4·SO3 და H2SO4·2SO3.
ოლეუმი ასევე შეიცავს პიროგოგირდმჟავას, რომელიც მიიღება შემდეგი რეაქციით:
გოგირდმჟავის წყალხსნარების დუღილის ტემპერატურა იზრდებამის კონცენტრაციის ზრდასთან ერთად და მაქსიმალურს აღწევს 98,3 % H2SO4-ის შემცველობისას.
| შემცველობა, მასური წილი % | სიმკვრივე 20 ℃-ზე, გრ/სმ³ | დნობის ტემპერატურა, ℃ | დუღილის ტემპერატურა, ℃ | |
|---|---|---|---|---|
| H2SO4 | SO3 (თავისუფალი) | |||
| 10 | - | 1,0661 | −5,5 | 102,0 |
| 20 | - | 1,1394 | −19,0 | 104,4 |
| 40 | - | 1,3028 | −65,2 | 113,9 |
| 60 | - | 1,4983 | −25,8 | 141,8 |
| 80 | - | 1,7272 | −3,0 | 210,2 |
| 98 | - | 1,8365 | 0,1 | 332,4 |
| 100 | - | 1,8305 | 10,4 | 296,2 |
| 104,5 | 20 | 1,8968 | −11,0 | 166,6 |
| 109 | 40 | 1,9611 | 33,3 | 100,6 |
| 113,5 | 60 | 2,0012 | 7,1 | 69,8 |
| 118,0 | 80 | 1,9947 | 16,9 | 55,0 |
| 122,5 | 100 | 1,9203 | 16,8 | 44,7 |
SO3-ის შემცველობის მომატებით ოლეუმის დუღილის ტემპერატურა მცირდება. გოგირდმჟავის წყალხსნარების კონცენტრაციის მომატებისას ხსნარებზე ორთქლის საერთო წნევა მცირდება და 98,3 % H2SO4-ის შემცველობისას აღწევს მინიმუმს. ოლეუმში SO3 კონცენტრაციის მომატებისას, ორთქლის საერთო წნევა ზედაპირზე იმატებს. გოგირდმჟავისა და ოლეუმის წყალხსნარების ზედაპირზე საერთო ორთქლის წნევა შეიძლება გამოითვალოს განტოლებით:
А და В კოეფიციენტების სიდიდეები დამოკიდებულია გოგირდმჟავის კონცენტრაციაზე. ორთქლი გოგირდმჟავის წყალხსნარებზე შედგება წყლის, H2SO4 და SO3 ნარევისაგან, ამასთან ორთქლის შემადგენლობა განსხვავდება გოგირდმჟავის ყველანაირი კონცენტრაციის სითხის შემადგენლობისაგან, გარდა შესაბამისი აზეოტროპული ნარევისა.
ტემპერატურის ზრდასთან ერთად ძლიერდება დისოციაცია:
გაწონასწორების კონსტანტის (გაწონასწორების მუდმივა) ტემპერატურული დამოკიდებულების განტოლება:
ნორმალური წნევისას დისოციაციის ხარისხი: 10⁻⁵ (373 К), 2,5 (473 К), 27,1 (573 К), 69,1 (673 К).
100%-იანი გოგირდმჟავის სიმკვრივე შეიძლება განისაზღვროს განტოლებით:
გოგირდმჟავის ხსნარების კონცენტრაციის ზრდასთან ერთად მათი თბოტევადობა მცირდება და მინიმუმს აღწევს 100%-იანი გოგირდმჟავისათვის. თბოტევადობა ოლეუმისათვის SO³-ის შემცველობის ზრდასთან ერთად იზრდება.
კონცენტრაციის მომატების და ტემპერატურის შემცირების დროს თბოგამტარობა λ მცირდება:
სადაც С — გოგირდმჟავის კონცენტრაცია, %-ში.
მაქსიმალური სიბლანტე აქვს ოლეუმს H₂SO₄·SO₃, ტემპერატურის მომატებით η მცირდება. გოგირდმჟავის ელექტრო წინაღობა მინიმალურია SO₃-სა და 92 % H₂SO₄-ის კონცენტრაციის დროს და მაქსიმალურია 84 და 99,8 % H₂SO₄კონცენტრაციის დროს. ოლეუმისათვის მინიმალურია ρ 10 % SO₃ კონცენტრაციისას. გოგირდმჟავის ტემპერატურის ზრდასთან ერთად ρ იზრდება. დიელექტრიკული შეღწევადობა 100%-იან მჟავისათვის არის 101 (298,15 К), 122 (281,15 К); კრიოსკოპიული მუდმივა - 6,12, ებულიოსკოპიური მედმივა - 5,33; გოგირდმჟავის ორთქლის დიფუზიის კოეფიციენტი ჰაერში იცვლება ტემპერატურასთან ერთად; D = 1,67·10⁻⁵T3/2 სმ²/წმ.
ქიმიური თვისებები
[რედაქტირება | წყაროს რედაქტირება]გოგირდმჟავა — საკმაოდ ძლიერი მჟანგავია, განსაკუთრებულად გახურებისას და კონცენტრირებული სახით; ჟანგავს HI და ნაწილობრივ HBr თავისუფალ ჰალოგენებამდე, ნახშირბადს CO2-მდე, S — SO2-მდე, ჟანგავს ბევრ ლითონს (Cu, Hg და სხვას). ამასთან გოგირდმჟავა ღდგება SO2-მდე, ხოლო ყველაზე ძლიერ აღმდგენებთან — S-მდე და H2S-მდე. კონცენტრირებული H2SO4 ნაწილობრივ ღდგება წყალბადით, რის გამოც არ შეიძლება გამოყენებულ იქნას მის გასაშრობად. განზავებული H2SO4 ურთიერთქმედებს ყველა ლითონთან, რომლებიც ელექტროქიმიურ დაძაბულობის რიგში დგანან წყალბადის მარცხნივ, წყალბადის გამოყოფით. მჟანგავი თვისებები განზავებული H2SO4-ისათვის არადამახასიათებელია. გოგირდმჟავა წარმოქმნის მარილების ორ რიგს: საშუალო — სულფატები და მჟავე — ჰიდროსულფატებს, და ასევე ეთერებს. ცნობილია პეროქსომონოგოგირდმჟავა (ან კაროს მჟავა) H2SO5 და პეროქსოდიგოგირდმჟავა H2S2O8.
გამოყენება
[რედაქტირება | წყაროს რედაქტირება]გოგირდმჟავა გამოიყენება:
- მინერალური სასუქების წარმოებაში;
- როგორც ელექტროლიტი ტყვიის აკუმულატორებში;
- სხვადასხვაგვარი მინერალური მჟავეებისა და მარილების მისაღებად;
- ქიმიური ბოჭკოების, საღებავების, კვამლწარმომქმნი და ასაფეთქებელი ნივთიერებების წარმოებისათვის;
- მრეწველობის ნავთობის, ლითონდამმუშავებელ, ტექსტილის, ტყავის და სხვა გადამამუშავებელ დარგებში;
- კვების მრეწველობაში — დარეგისტრირებულია როგორც საკვები დანამატი E513(ემულგატორი);
- სამრეწველო ორგანულ სინთეზში რეაქციებში:
- დეჰიდრატაცია (დიეთილის ეთერის მიღებისას, რთულ ეთერებში);
- ჰიდრატაციაში (ეთილენიდან ეთანოლში);
- სულფირებაში (სინთეთიკური სარეცხი საშუალებები და საღებავების წარმოებაში როგორც შუალედური პროდუქტები);
- ალკილირება (იზოოქტანების მიღება, პოლიეთილენგლიკოლის, კაპროლაქტამი) და სხვა.
- ფისების აღსადგენად ფილტრებში დისტილირებული წყლის წარმოებაში.
გოგირდმჟავის მსოფლიო წარმოება არის მიახლოებით 160 მლნ ტონა წელიწადში. ყველაზე მსხვილი მომხმარებელია - მინერალური სასუქების ცარმოება. 1 ტ P₂O₅ ფოსფორულ სასუქებზე იხარჯება 2,2-3,4 ტ გოგირდმჟავა, ხოლო 1 ტ (NH₄)₂SO₄ — 0,75 ტ გოგირდმჟავა. ამიტომაც გოგირდმჟავის ქარხნებს ცდილობენ ააგონ მინერალური სასუქების ქარხნებთან ერთად კომპლექსში.
ტოქსიკური ქმედება
[რედაქტირება | წყაროს რედაქტირება]გოგირდმჟავა და ოლეუმი - ძალიან საშიში ნივთიერებებია. ისინი აზიანებენ კანს, ლორწვან გარსს, სასუნთქ გზებს (იწვევს ქიმიურ დამწვრობას). ამ ნივთიერებების ორთქლის ჩასუნთქვისას ისინი იწვევენ სუნთქვის გაძნელებას, ხველებას, ხშირად — ლარინგიტს, ტრაქეიტს, ბრონქიტს და ა.შ. სამუშაო ზონაში ჰაერში გოგირდმჟავის აეროზოლის ზღვრული დასაშვები კონცენტრაცია არის 1,0 მგრ/მ³, ატმოსფეროს ჰაერში 0,3 მგრ/მ³ (მაქსიმალური ერთჯერადი) და 0,1 მგრ/მ³ (საშუალო დღეღამური). გოგირდმჟავის ორთქლის საზიანო კონცენტრაცია არის 0,008 მგრ/ლ (ექსპოზიცია 60 წთ), სასიკვდილო 0,18 მგრ/ლ (60 წთ). საშიშროების კლასი II. გოგირდმჟავის აეროზოლი შეიძლება წარმოიქმნას ატმოსფეროში ქიმიური და მეტალურგიული გამონაბოლქვების დროს, რომლებიც შეიცავენ S-ის ოქსიდებს, და მჟავის წვიმის სახით მოდის.
ისტორიული ცნობები
[რედაქტირება | წყაროს რედაქტირება]
გოგირდმჟავა უძველესი დროიდანაა ცნობილი, ბუნებაში თავისუფალი სახით, მაგალითად, ტბების სახით ვულკანებთან ახლოს [1]. სავარაუდოდ, პირველად მჟავა აირები მოხსენიებული აქვს არაბ ალქიმიკოსს ჯაბარ იბნ ჰაიანს რომელიც აღწერს მის მიღებას შაბიამნების ან რკინს სულფატების «რკინის ქვის» გახურებით.
IX საუკუნეში სპარსელმა ალქიმიკოსმა არ-რაზიმ, რკინისა და სპილენძის შაბიამნების ნარევის (FeSO4•7H2O და CuSO4•5H2O) გახურებისას, ასევე მიიღო გოგირდმჟავის ხსნარი. ეს მეთოდი უფრო დახვეწა ევროპელმა ალქიმიკოსმა ალბერტ მაგნუსმა, რომელიც XIII ს. ცხოვრებდა.
XV საუკუნეში ალქიმიკოსებმა აღმოაჩინეს, რომ გოგირდმჟავა შეიძლება მიღებულ იქნას, გოგირდის და გვარჯილის ნარევის დაწვით, ან გოგირდის კოლჩედანისაგან - პირიტისაგან, უფრო იაფი და გავრცელებული ნედლეულისაგან ვიდრე არის გოგირდი. ამ მეთოდით მიიღებდნენ გოგირდმჟავას 300 წლის განმავლობაში, მცირე რაოდენობებით მინის რეტორტებში. და მხოლოდ მე-18 საუკუნეში, როდესაც დადგენილ იქნა, რომ ტყვია არ იხსნება გოგირდმჟავაში, მინის ლაბორატორიული ჭურჭელიდან გადავიდნენ სამრეწველო ტყვიის კამერებზე.
დამატებითი ცნობები
[რედაქტირება | წყაროს რედაქტირება]გოგირდმჟავის მწვრილი წვეთები შეიძლება წარმოიქმნას შუა და ზედა ატმოსფეროში წყლის ორთქლისა და ვულკანური ფერფლის (რომელიც შეიცავს გოგირდის დიდ რაოდენობას) რეაქციის შედეგად. რის გამოც ჭირს მზის სხივების მოხვედრა პლანეტის ზედაპირზე. ამან (ასევე ვულკანური ფერფლის მცირე ნაწილაკების დიდმა რაოდენობამ ატმოსფეროს ზედა ფენებში, ამცირებენ მზის სხივების მოხვედრას დედამიწის ზედაპირზე) განსაკუთრებულად დიდი ვულკანის ამოფრქვევის დროს შეიძლება გამოიწვიოს კლიმატის ცვლილება. მაგალითად, ვულკან კსუდაჩის (კამჩატკის ნახევარკუნძული) ამოფრქვევის შედეგად 1907 წ.) ფერფლისა და მტვერის ჭარბი კონცენტრაცია ატმოსფეროში მიახლოებით 2 წლის განმავლობაში იყო, ხოლო გოგირდმჟავის დამახასიათებელი მოვერცხლისფრო ღრუბლები შეიმჩნეოდა პარიზშიც კი[2]. ვულკან პინატუბოს აფეთქებამ 1991 წ. რომელმაც ატმოსფეროში ამოაფრქვია 3×107 ტონა გოგირდი, მიიყვანა იქამდე, რომ 1992 და 1993 წლები ოყო მნიშვნელოვნად უფრო ცივი იყო ვიდრე 1991 და 1994 [3].
გოგირდმჟავის მიღება
[რედაქტირება | წყაროს რედაქტირება]გოგირდმჟავა ქიმიური მრეწველობის უმნიშვნელოვანესი პროდუქტია. დღეისთვის მას აწარმოებენ კონტაქტური მეთოდით. აღნიშნული მეთოდით გოგირდმჟავას წარმოება სტადიებად მიმდინარეობს. პირველ სტადიაზე ხდება გოგირდოვანი ანჰიდრიდის მიღება, ნედლეულად კი იყენებენ პირიტს- FeS2, პირიტს წინასწარ დააქუცმაცებენ განსაკუთრებული ზომის ნაწილაკამდე, ჩატვირთავენ სპეციალურ ღუმელებში,რომელშიც ქვემოდან ცხელ ჰარეს უბერავენ. ღუმელში წარმოიქმნება ე.წ "მდუღარე შრე" და გამოწვა სწრაფად ხდება:
- 4FeS2+ 11O2 → 2Fe2O3 + 8SO2
ღუმელიდან გამომავალი SO2 უამრავ მინარებს და მტვერს შეიცავს. მას ღუმელის გაზი ეწოდება, მას გაატარებენ სპეციალურ დანადგარებში გასასუფთავებლად და გასაშრობად, პირველად გაივლის ელექტროფილტრში, აქედან კი საშრობ კოშკში. მისი გაშრობა ხდება კონცენტრირებული გოგირდმჟავათი. აქ ღუმელის გაზი და გოგირდმჟავა მოძრაობს ურთიერთსაპირისპირო მიმართულებით, რომელსაც წინაღდგენი პრინციპი ეწოდება. საშრობი კოშკიდან გოგირდოვანი გაზი მიეწოდება საკონტაქტო აპარატს,რომელშიც მოთავსებულია ე.წ კატალიზატორის კოლოგი, რომელშიც კატალიზატორად იყენებენ პლატინის ან ვანადიუმის (V) ოქსიდს. გოგირდოვანი გაზის დაჟანგვა შექცევადი პროცესია. სითბოს გამოყოფით მიმდინარეობს და საჭირო ხდება ოპტიმალური პირობების დაცვა SO2-ის გამოსავლიანობის გადიდების მიზნით
- 2SO2 + O2 → 2SO3 + Q
ტემპერატურული რეჟიმია 450-600° , ამ ტემპერატურული რეჟიმის შესანარჩუნებლად გამოყენებულია ამ რეაქციაში წარმოშობილი სითბო, რის გამოც მიღებულ პროდუქტს თბოგადამცემში (მაცივარში) ატარებენ, ნაჭარბი სითბო აპარატში შესასვლელი ნარევის გათბობას ხმარდება. აღნიშნულ პრინციპს თბოგადაცემის პრინციპი ეწოდება. მესამე სტადიაზე ხდება გოგირდმჟავას მიღება
- SO3 + H2O → H2SO4 + Q
აღნიშნული რეაქცია ეგზოთერმულია, ამის გამო მშთანთქმელ კოშკში ნისლი წარმოიქმნება და პროცესი წყდება, ამიტომ კოშკში ზემოდან ასხამენ არა წყალს, არამედ განზავებულ გოგირდმჟავას (საშრობი კოშკიდან მოდის) შედეგად მიღება ძლიერ კონცენტრირებულ გოგირდმჟავა - ოლეუმი, რომლის წყლთ განზავებისას მიიღება სასურველი კონცენტრაციის გოგირდმჟავა. ოლეუმის გაცივებისას მისგან გამოიყოფა პიროგოგირდმჟავა
- SO3 + H2SO4 → H2S2O7
- H2S2O7 + H2O → 2H2SO4
ლიტერატურა
[რედაქტირება | წყაროს რედაქტირება]- ქართული საბჭოთა ენციკლოპედია, ტ. 3, თბ., 1978. — გვ. 198.
- მეგოგირდმჟავის ცნობარი, რედ. კ. მ. მალინა, 2 გამოც., მ., 1971
რესურსები ინტერნეტში
[რედაქტირება | წყაროს რედაქტირება]სქოლიო
[რედაქტირება | წყაროს რედაქტირება]- ↑ დაარქივებული ასლი. დაარქივებულია ორიგინალიდან — 2012-04-25. ციტირების თარიღი: 2012-04-03.
- ↑ იხ. სტატია «Вулканы и климат» დაარქივებული 2007-09-28 საიტზე Wayback Machine. (რუსული)
- ↑ Русский архипелаг — Виновато ли человечество в глобальном изменении климата? (რუსული)







