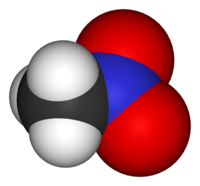
ნიტრომეთანი
| ნიტრომეთანი | |
 | |
 | |
| ზოგადი | |
|---|---|
| სისტემური სახელწოდება | ნიტრომეთანი[1] |
| ტრადიციული სახელწოდება | ნიტროკარბოლი |
| ქიმიური ფორმულა | |
| მოლური მასა | 61.04 გ/მოლი |
| ფიზიკური თვისებები | |
| სიმკვრივე | 1.1371(20 °C)[2] გ/სმ³ |
| თერმული თვისებები | |
| დნობის ტემპერატურა | −28.7[2] °C |
| დუღილის ტემპერატურა | 101.2[2] °C |
| ქიმიური თვისებები | |
| pKa | 17.2[3] |
| სტრუქტურა | |
| დიპოლური მომენტი | 3.46[4] დ |
ნიტრომეთანი — ორგანული ნივთიერება ქიმიური ფორმულით . არის უმარტივესი ორგანული ნიტრონაერთი, მწარე ნუშის სუნის მქონე უფერული სითხე. გამოიყენება გამხსნელად, არომატული ნახშირწყალბადების ექსტრაქციისათვის, ქლორპიკრინის,[5] ფარმაცევტული საშუალებების, პესტიციდების, ასაფეთქებელი ნივთიერებების, ბოჭკოების და საიზოლაციო მასალების დასამზადებლად[6]. მას ასევე იყენებენ როგორც საწვავის დანამატს.
დუღილის ტემპერატურა 101,2°C, სიმკვრივე 1138 კგ/მ³ (20°C); წყალში იხსნება; ერევა ჩვეულებრივ ორგანულ გამხსნელებს (პარაფინების გარდა), წყალთან წარმოქმნის აზეოტროპულ ნარევს (tდუღ 83,6°C, 76,4% ნიტრომეთანი).[5]
მიღება[რედაქტირება | წყაროს რედაქტირება]
ინდუსტრიული მეთოდი[რედაქტირება | წყაროს რედაქტირება]
- ნიტრომეთანი ინდუსტრიულად იწარმოება აირად ფაზაში მყოფი პროპანისა და აზოტმჟავასგან 350–450 °C-ის პირობებში. ეს ეგზოთერმული რეაქცია წარმოქმნის ოთხ ინდუსტრიულად მნიშვნელოვან ნიტროალკანს: ნიტრომეთანს, ნიტროეთანს, 1-ნიტროპროპანს და 2-ნიტროპროპანს.[6]
ლაბორატორიული მეთოდი[რედაქტირება | წყაროს რედაქტირება]
- ლაბორატორიაში ნიტრომეთანის მიღება ხდება ნატრიუმის ქლორაცეტატის და ნატრიუმის ნიტრიტის ურთიერთქმედებით ხსნარში.[7]
- ClCH2COONa + NaNO2 + H2O → CH3NO2 + NaCl + NaHCO3
სქოლიო[რედაქტირება | წყაროს რედაქტირება]
- ↑ (2014) „Front Matter“, Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry, გვ. 662. DOI:10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
- ↑ 2.0 2.1 2.2 Haynes, p. 3.414
- ↑ Reich, Hans. Bordwell pKa table: "Nitroalkanes". ციტირების თარიღი: 17 January 2016.
- ↑ Haynes, p. 15.19
- ↑ 5.0 5.1 ქართული საბჭოთა ენციკლოპედია, ტ. 7, თბ., 1984. — გვ. 445.
- ↑ 6.0 6.1 Markofsky, S. B. (2000). „Nitro Compounds, Aliphatic“. Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a17_401.pub2. ISBN 978-3527306732.
- ↑ Whitmore, F. C.; Whitmore, M. G. (1941). "Nitromethane". Organic Syntheses.; Collective Volume, 1, p. 401

