ამონიუმი: განსხვავება გადახედვებს შორის
| [შემოწმებული ვერსია] | [შემოწმებული ვერსია] |
შიგთავსი ამოიშალა შიგთავსი დაემატა
No edit summary |
No edit summary |
||
| ხაზი 77: | ხაზი 77: | ||
| NFPA 704 = <!-- (აშშ-ის სტანდარტი, ხანძარსაწინააღმდეგო დაცვის ეროვნული ასოციაცია) --> |
| NFPA 704 = <!-- (აშშ-ის სტანდარტი, ხანძარსაწინააღმდეგო დაცვის ეროვნული ასოციაცია) --> |
||
}} |
}} |
||
'''ამონიუმი''' — [[კატიონი |
'''ამონიუმი''' — [[კატიონი]] <chem>NH_4+</chem>, შედის მრავალი ნაერთის შემადგენლობაში, სადაც ერთვალენტოვანი [[ლითონი|ლითონის]] როლს ასრულებს. ასეთებია [[ამონიუმის ჰიდროქსიდი]] და ამონიუმის მარილები: [[ამონიუმის სულფატი]], [[ამონიუმის ქლორიდი]] და სხვ. ამონიუმის მარილების უმეტესობა უფერო კრისტალური, წყალში კარგად ხსნადი ნივთიერებებია, გახურებისას ადვილად იშლებიან [[ამიაკი|ამიაკის]] გამოყოფით. წყალხსნარებში ამონიუმის ნაერთების დისოციაციის დროს ამონიუმი [[კატიონი|კატიონის]] სახითაა, მაგ.: |
||
:<chem>NH_4Cl \rightleftarrows NH_4 + Cl^-</chem> |
:<chem>NH_4Cl \rightleftarrows NH_4 + Cl^-</chem> |
||
17:45, 26 დეკემბერი 2019-ის ვერსია
 | |
 | |
| ზოგადი | |
|---|---|
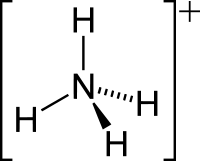
| სისტემური სახელწოდება | ამონიუმი აზანიუმი[1] |
| ქიმიური ფორმულა | |
| მოლური მასა | 18.039 გ/მოლი |
| ქიმიური თვისებები | |
| pKa | 9.25 |
ამონიუმი — კატიონი , შედის მრავალი ნაერთის შემადგენლობაში, სადაც ერთვალენტოვანი ლითონის როლს ასრულებს. ასეთებია ამონიუმის ჰიდროქსიდი და ამონიუმის მარილები: ამონიუმის სულფატი, ამონიუმის ქლორიდი და სხვ. ამონიუმის მარილების უმეტესობა უფერო კრისტალური, წყალში კარგად ხსნადი ნივთიერებებია, გახურებისას ადვილად იშლებიან ამიაკის გამოყოფით. წყალხსნარებში ამონიუმის ნაერთების დისოციაციის დროს ამონიუმი კატიონის სახითაა, მაგ.:
მჟავა-ფუძე თვისებები
ამონიუმის იონი მიიღება, როდესაც ამიაკი, როგორც მცირე ფუძე თვისებების მქონე, რეაქციაში შევა პროტონთან.
- H+ + NH3 → NH4+
ლიტერატურა
- ქართული საბჭოთა ენციკლოპედია, ტ. 1, თბ., 1975. — გვ. 402.
სქოლიო
- ↑ International Union of Pure and Applied Chemistry (2005). Nomenclature of Inorganic Chemistry (IUPAC Recommendations 2005). Cambridge (UK): RSC–IUPAC. ISBN 0-85404-438-8. pp. 71,105,314. Electronic version.


